程立立,刘少华,刘珊,许鹏宇,李冬秀,刘秀萍,刘松娜,齐丽丽
(1.河北医科大学第三医院,石家庄 050000;
2.邢台医学高等专科学校第一附属医院,邢台 054000;
3.中国人民解放军联勤保障部队第九八○医院,石家庄 050000)
目前,关于胚胎反复种植失败(RIF)并没有一个普遍接受的定义,较公认的定义为:经历3次及以上移植周期,且累积移植卵裂期优质胚胎数目不少于4枚或高评分囊胚2枚而未获得临床妊娠者[1]。胚胎着床是一个复杂的过程,其中胚胎质量和子宫内膜容受性是成功着床的两个重要因素[2]。对于RIF患者而言,最主要的影响因素是子宫内膜容受性。因此,改善子宫内膜容受性对于改善RIF患者的妊娠结局具有重要意义,是辅助生殖领域的研究热点和难点。宫腔灌注是目前临床上改善子宫内膜容受性的常用方法,灌注药物多种多样,包括粒细胞集落刺激因子(G-CSF)、人绒毛膜促性腺激素(HCG)及地塞米松磷酸钠注射液(DexSPI)等,对子宫内膜厚度、胚胎种植率及临床妊娠率均有明显提高。但是关于不同的灌注物之间是否存在治疗差异鲜有研究。本研究拟探讨宫腔灌注G-CSF、DexSPI和HCG对子宫内膜和妊娠结局的影响,以期找到有效的改善子宫内膜容受性的方法,提高胚胎着床率及临床妊娠率。
一、研究对象
回顾性分析2018年5月至2021年10月于中国人民解放军联勤保障部队第九八○医院生殖中心接受冻融胚胎移植(FET)治疗并行宫腔灌注的120例RIF患者的临床资料。纳入标准:(1)本周期采用激素替代方案准备内膜;
(2)本次移植至少有1枚优质卵裂胚。排除标准:(1)年龄≥38岁;
(2)宫腔灌注前内膜厚度<7 mm;
(3)存在其他影响胚胎着床的因素,如子宫畸形、子宫内膜异位症、子宫腺肌症、子宫内膜息肉、子宫内膜炎、输卵管积水以及宫腔粘连等;
(4)存在某些其他的合并症,如凝血功能异常,免疫系统异常等。
根据宫腔灌注药物不同分为3组:宫腔灌注HCG的HCG组(44例),宫腔灌注G-CSF的G-CSF组(42例),宫腔灌注G-CSF+DexSPI的G-CSF+DexSPI组(34例)。选择同期行激素替代周期准备内膜、仅行FET(未行宫腔灌注)的36例患者为对照组。
二、研究方法
1.内膜准备:采用激素替代方案准备内膜。患者于月经第2~3天开始口服戊酸雌二醇(补佳乐,拜耳,德国)6~8 mg/d,7 d后返院。根据内膜厚度及血清激素水平调整补佳乐剂量,于用药的16~18 d、子宫内膜厚度≥8 mm、E2>734 pmol/L时,给予雪诺酮(默克雪兰诺,德国)90 mg/d+地屈孕酮(雅培,荷兰)20 mg/d或者安琪坦(法杏大药厂,法国)400 mg/d+地屈孕酮20 mg/d转化子宫内膜,4 d后移植解冻复苏的卵裂胚。
2.宫腔灌注液的配制:(1)HCG组:用2 ml的生理盐水溶解2 000 U的HCG(珠海丽珠),混合均匀后抽取0.5 ml的液体,即500 U的HCG备用;
(2)G-CSF组:将G-CSF(吉赛欣,石家庄华北制药)150 μg(0.6 ml)抽吸入1 ml的注射器内备用;
(3)G-CSF+DexSPI组:将G-CSF 75 μg(0.3 ml)和DexSPI(地塞米松磷酸钠注射液,天津金耀)5 mg(1 ml)抽吸入2 ml的注射器内备用。
3.宫腔灌注的方法:于子宫内膜转化日(移植前4 d)行宫腔内灌注,嘱患者排空膀胱,取膀胱截石位。常规消毒外阴,铺无菌洞巾,窥器暴露宫颈,生理盐水棉球擦拭阴道和宫颈。用注射器吸取灌注液,与一次性无菌人工授精管相连接,将人工授精管置入宫腔,缓慢将药液注入宫腔,停留数秒后取出人工授精管。嘱患者卧床休息30 min。
4.卵裂胚质量的评估:根据卵裂球数目[第3日(D3)胚胎的卵裂球数目≥6细胞]、形态和胞浆中的碎片等将胚胎分为4级[3]。Ⅰ级:胚胎卵裂球形态规则,大小均匀,透明带完整,胞质均匀清晰,碎片无或少于5%;
Ⅱ级:胚胎卵裂球形态略不规则,大小略不均,胞质可有颗粒现象,碎片10%~20%;
Ⅲ级:胚胎卵裂球大小明显不均匀,可有明显的形态不规则,胞质可有颗粒现象,碎片21%~50%;
Ⅳ级:胚胎卵裂球大小严重不均,胞质可有严重颗粒现象,碎片大于50%。结合本实验室实际情况,本研究优质胚胎评定标准为:取卵后D3胚胎评分为Ⅰ、Ⅱ级,7个≤卵裂球≤9个、排列规则、碎片≤20%的胚胎。
5.黄体支持与随访:所有胚胎均采用玻璃化冷冻,复苏后选择至少1个优质胚胎进行移植,给予常规黄体支持(雪诺酮90 mg/d或者安琪坦400 mg/d+地屈孕酮20 mg/d),移植后14 d查血β-HCG,若β-HCG>50 U/L为阳性;
阳性者移植后30 d行B超检查,观察到妊娠囊或胎心搏动为临床妊娠,随访至胚胎移植后70 d。
三、统计学分析

一、各组一般情况比较
4组患者间平均年龄、不孕年限、体质量指数(BMI)、基础卵泡刺激素(bFSH)、基础黄体生成素(bLH)及基础雌二醇(bE2)水平比较,差异均无统计学意义(P>0.05)(表1)。

表1 各组患者一般情况比较(-±s)
二、各组胚胎移植和内膜情况比较
4组患者间既往移植失败周期数及移植失败周期优胚数均无统计学差异(P>0.05)。本次移植胚胎数、优胚数、转化日内膜厚度及胚胎移植日内膜厚度之间均无显著差异性(P>0.05)(表2)。

表2 各组患者胚胎移植和内膜情况比较(-±s)
三、各组妊娠结局比较
HCG组、G-CSF组及G-CSF+DexSPI组患者本周期的胚胎着床率、临床妊娠率均显著高于对照组(P<0.05),而3组患者间比较均无统计学差异(P>0.05)。4组患者间早期流产率、异位妊娠率比较均无统计学差异(P>0.05)(表3)。
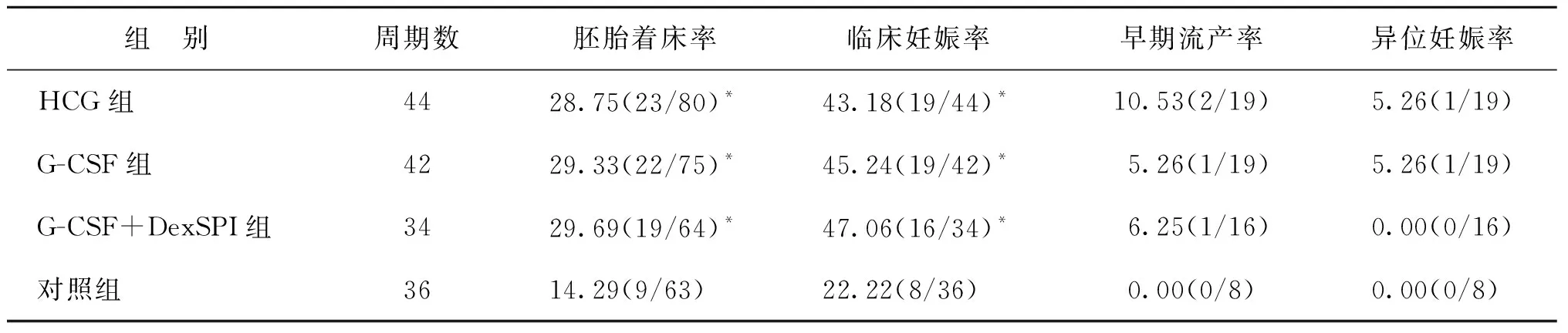
表3 各组患者妊娠结局比(%)
目前,体外受精-胚胎移植(IVF-ET)成为不孕患者成功妊娠的主要手段。随着控制性卵巢刺激(COS)方案的不断完善、胚胎实验室设备及技术的不断提高,IVF/ICSI周期的胚胎着床率、临床妊娠率均得到了显著提高,但仍有部分患者出现RIF。对于RIF患者来说,子宫内膜容受性是影响胚胎着床的重要因素之一[4]。
子宫内膜容受性又称着床窗口期,是子宫内膜接纳容受胚胎的一种能力,是允许胚胎黏附、穿透并侵入的一种状态[5-6],其机制复杂。目前,对于子宫内膜容受性的研究较多,有药物治疗、子宫内膜搔刮及宫腔灌注等[7-10]。其中宫腔灌注是近年来出现的一种新型治疗方法,是将某些药物或细胞因子于特定时期经宫颈内口缓慢注入宫腔内以改善内膜状况的一种方法,是相对无创的一种治疗方法。一般是在胚胎移植前1~3 d进行灌注,也有的研究于移植前1~2 h进行灌注。灌注的药物主要有G-CSF、HCG、生长激素(GH)、DexSPI、自体外周血单个核细胞(PBMCs)等。
在子宫内膜种植窗期,有多种细胞及体液因子的参与,其中HCG的作用至关重要[11]。HCG是胚胎种植前分泌的一种早期信号分子,可以启动、控制胎盘绒毛膜细胞侵袭、种植,在胚胎着床、妊娠中发挥着重要的作用。有研究报道,宫腔内灌注HCG可上调胚胎植入的相关蛋白,有利于胚胎种植,显著提高临床妊娠率[12]。
Gao等[13]的一篇纳入15项随机对照试验(RCT)的Meta分析研究结果表明,移植前宫腔灌注HCG,不但能提高胚胎种植率、临床妊娠率及胎儿出生率,还能降低流产率。张乐等[14]的一项Meta分析也表明,灌注组与对照组相比,胚胎种植率与临床妊娠率差异均有统计学意义(P<0.05)。但也有研究结果显示,行FET前宫腔内灌注500 U HCG并不明显提高妊娠率[15]。
在生殖系统中,G-CSF由颗粒细胞产生,参与卵泡的生长发育、排卵以及妊娠等多个环节。宫腔灌注G-CSF,可以使内膜组织血流信号增加,刺激子宫内膜细胞的增生,促进子宫内膜的修复与生长,促进内源性细胞因子的分泌,改善子宫内膜容受性,使胚胎种植率增加;
宫腔灌注G-CSF,还可抑制子宫内膜炎症。张曦倩等[16]研究发现,RIF患者于移植前宫腔灌注G-CSF,通过调节子宫内膜局部辅助T淋巴细胞,使Th1/Th2与Th17/Treg达到平衡,从而提高胚胎种植率和临床妊娠率。甘永安等[17]的一项纳入宫腔灌注G-CSF的840个周期的Meta分析表明,宫腔灌注G-CSF患者的胚胎种植率、临床妊娠率均显著高于对照组(P<0.05),但两组间排卵日子宫内膜厚度无统计学差异(P>0.05)。白春梅等[18]的研究结果表明,宫腔灌注G-CSF能增加薄型子宫内膜患者FET周期中子宫内膜厚度、胚胎种植率和临床妊娠率,降低周期取消率。而Lian等[19]的一项研究发现,对于RIF患者,宫腔灌注G-CSF虽然可增加子宫内膜厚度,但患者的胚胎种植率无明显增加。另一项研究也表明,对于子宫内膜厚度正常的RIF患者,宫腔灌注G-CSF不能增加患者的子宫内膜厚度及胚胎种植率[20]。
本研究选取子宫内膜转化日行宫腔灌注的RIF患者作为研究对象进行分析,结果显示,宫腔灌注HCG及G-CSF不增加子宫内膜厚度,但可以改善子宫内膜容受性,使胚胎着床率和临床妊娠率显著增高(P<0.05),同时不增加流产率及异位妊娠率,与之前大多数学者们的研究结果相一致。
地塞米松是一种糖皮质激素,作用于T淋巴细胞与B淋巴细胞,抑制炎性因子的分泌及聚集[21-22],同时抑制自然杀伤(NK)细胞的活性,起到免疫调节作用。地塞米松广泛应用于自身免疫性疾病和移植后的排斥反应。Zhang等[23]研究指出,RIF与子宫自然杀伤细胞(uNK)有关,对于宫腔内高uNK导致RIF的患者,宫腔灌注地塞米松能够下调uNK的比例,从而改善子宫内膜的容受性,提高妊娠率。近年来越来越多的研究发现,宫腔灌注地塞米松用于uNK细胞比例异常的RIF患者,可以明显改善妊娠结局;
对于宫腔镜检查提示有慢性子宫内膜炎的RIF患者,宫腔灌注抗生素+地塞米松的治疗较单纯灌注抗生素效果显著,认为地塞米松能改善宫腔内局部免疫环境[24-25]。
本研究选取单纯行G-CSF灌注及G-CSF+DexSPI灌注的患者进行比较,结果显示,FET前内膜转化日行宫腔灌注G-CSF+DexSPI患者的胚胎着床率及临床妊娠率均显著高于对照组(P<0.05);
胚胎着床率及临床妊娠率稍高于G-CSF组,但无统计学差异(P>0.05)。与之前学者用地塞米松对子宫内膜NK细胞异常及慢性子宫内膜炎的RIF患者治疗效果一致。
本研究对不同的灌注药物对妊娠结局的影响进行比较,且入组患者全部采用激素替代方案进行内膜准备,排除了方案不同对妊娠率的影响,使结果更加可靠。本研究在实验组间也进行了比较,HCG组、G-CSF组及G-CSF+DexSPI组3组间的胚胎着床率、临床妊娠率及早期流产率、异位妊娠率均无统计学差异(P>0.05)。提示对于RIF患者来说,这3种宫腔灌注方案均可选择,可提高胚胎着床率及临床妊娠率。
综上所述,对于RIF患者,通过宫腔灌注HCG、G-CSF或G-CSF+DexSPI可以改善子宫内膜容受性,提高胚胎着床率及临床妊娠率;
且宫腔灌注通过局部给药,可使药物在局部达到更高的浓度,全身不良反应小,花费低,效果好。因此,临床可根据RIF患者具体情况,在这3种灌注方案中选择合适的灌注方法,改善子宫内膜容受性,提高妊娠率。