朱婧
胰腺癌首选治疗方法为手术,但其起病较为隐匿,具有高进展性,多数患者确诊时为晚期,癌细胞多已发生广泛转移,且胰腺癌晚期患者体质较差,难以耐受手术与麻醉创伤,因此丧失手术治疗的机会[1]。临床对于胰腺癌晚期患者常采取化疗、局部放疗等治疗方式。替吉奥为氟尿嘧啶类口服复合药物,具有抗肿瘤作用,为胰腺癌晚期一线化疗药物[2]。但胰腺癌进展迅速,单一药物作用疗效欠佳,需联合用药,以增强疗效。近年来,肿瘤分子靶向治疗药物不断发展,为胰腺癌的治疗提供了新的可能。尼妥珠单抗作为以表皮生长因子受体(epithelial growth factor receptor,EGFR)为靶点的人源化单抗药物,可阻断ECF-EGFR信号转导通路,抑制肿瘤细胞增殖[3]。结合上述药物作用机制,推测将尼妥珠单抗与替吉奥联合应用于胰腺癌晚期患者中或可提高收益。基于此,本研究观察尼妥珠单抗联合替吉奥在胰腺癌晚期患者中应用效果,并对有效性和安全性进行分析,以期为临床治疗方案的选取提供参照,报道如下。
1.1 一般资料 选取2017年1月至2021年1月江苏省属海安市人民医院收治的68例胰腺癌晚期患者作为研究对象,患者已签署知情同意书。估算本研究所需样本量,取α=0.05,β=0.1,标准差σ为1.57;
对照组与观察组平均值差值δ=1.21,计算得出每组样本量N1=N2=28,依据失访率20%计算,实际研究中,观察组与对照组各需34例,总需68例患者。再利用计算机生成的随机数字分成2组,每组34例。对照组中,男24例,女10例;
年龄45~75岁,平均年龄(58.74±4.39)岁;
体重指数18.56~25.63 kg/m2,平均(22.24±1.17)kg/m2;
病程2~21个月,平均病程(9.23±1.34)个月;
肿瘤部位:胰头24例,胰体尾8例,胰颈2例;
TNM分期:Ⅲb期11例,Ⅳ期23例。观察组中男22例,女12例;
年龄44~74岁,平均年龄(59.26±4.97)岁;
体重指数18.42~25.71 kg/m2,平均(22.03±1.09)kg/m2;
病程3~20个月,平均病程(9.84±1.47)个月;
肿瘤部位:胰头23例,胰体尾8例,胰颈3例;
TNM分期:Ⅲb期14例,Ⅳ期20例。2组一般资料比较差异无统计学意义(P>0.05)。
1.2 纳入与排除标准
1.2.1 纳入标准:①符合《胰腺癌诊疗指南(2014)》[4]中胰腺癌诊断标准;
②生存期临床预测>3个月;
③胰腺占位或胰腺转移病灶最大直径≥1 cm或病灶数≥1个;
④TNM分期[1]为Ⅲb期、Ⅳ期;
⑤认知功能正常,可配合完成本研究。
1.2.2 排除标准:①合并有心血管、脑血管、肝、肾或造血系统等严重原发性疾病;
②既往有精神病史;
③合并肝癌、胆囊癌等恶性肿瘤疾病;
④近1个月内接受过抗肿瘤治疗;
⑤严重的骨髓抑制;
⑥对尼妥珠单抗、替吉奥及其代谢物过敏;
⑦因自动出院、转科、转院等特殊原因,中途退出治疗。
1.3 治疗方法
1.3.1 对照组:使用替吉奥胶囊(齐鲁制药有限公司,治疗,口服给药,40 mg/次,2次/d,连续给药4周后休息2周,连续治疗6个月。
1.3.2 观察组:于对照组基础上,将100 mg的尼妥珠单抗注射液(百泰生物药业有限公司,与250 ml 0.9%氯化钠溶液充分混合后,以静脉输液的形式给药,单次给药时间应持续>1 h,给药过程密切观测患者身体状况,1周/次,连续治疗8周。
1.4 评价指标
1.4.1 临床疗效:参照相关标准[5],①完全缓解:肿瘤病灶全部消失,并于4周后复测证实;
②部分缓解:肿瘤病灶最大垂直径与横径乘积之和减少>50%或最大径之和减少>50%,并于4周后复测证实,多病灶时无需全部病灶均缩小>50%;
③稳定:肿瘤病灶最大垂直径与横径乘积之和减少>50%,或增加25%,未出现新病灶,并于4周后复测证实;
④进展:至少1个病灶双径乘积或单径增加>25%,或有新病灶萌出。临床收益率=(完全缓解例数+部分缓解例数+稳定例数)/总例数×100%。
1.4.2 毒副反应:于治疗期间,统计2组发生的毒副反应,并应用抗肿瘤药物不良反应的分度标准[5]对治疗期间出现的毒副反应进行分级,分为0~Ⅳ度。
1.4.3 生存情况:对2组患者进行12个月的随访,统计并比较2组随访期间的生存状况(生存/病死)以及生存时间(以病死为终点事件)。
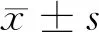
2.1 2组临床疗效比较 观察组临床收益率(67.65%)明显高于对照组(41.18%),差异有统计学意义(P<0.05)。见表1。

表1 2组患者临床疗效比较 n=34,例(%)
2.2 2组毒副反应比较 观察组白细胞减少、血红蛋白减少、中性粒细胞减少、恶心呕吐、腹泻、食欲下降等毒副反应略高于对照组,但差异无统计学意义(P>0.05)。见表2。

表2 2组患者毒副反应比较 例(%)
2.3 生存情况 随访12个月,结果显示,对照组中位生存时间估计值为5个月(95%CI:3.961~6.039),观察组中位生存时间估计值为7个月(95%CI:5.581~8.419),运用Log rank法对胰腺癌晚期患者生存时间的差异进行检验,结果显示,观察组总体生存时间高于对照组(χ2=4.040,P=0.044)。见图1。

图1 2组患者生存函数图
胰腺癌的发生与长期吸烟、肥胖、胰腺慢性疾病等因素密切相关,患者病情进展十分迅速,确诊时病情多已发展至晚期,此时已发生淋巴结转移和远处转移,以至于大部分的患者失去手术指征,即使部分局部晚期胰腺癌患者可接受手术治疗,但术后仍具有较高的复发率和转移率,预后较差[6]。因此,进行科学、合理的药物治疗,对延长晚期胰腺癌患者生存期十分必要。替吉奥常被临床用于治疗晚期胰腺癌患者,为抗代谢化疗药物,可抑制肿瘤细胞增殖,虽取得一定疗效,但患者生存期仍较短[7]。随着分子生物学、基因组织学的发展,临床研究重点向肿瘤微环境内的成分、相关信号转导途径转移,其中EGFR为重点关注对象[8]。临床研究显示,胰腺癌细胞向四周浸润和远处转移过程中EGFR信号通路呈现异常激活状态,选择性的对EGFR信号通路进行阻断,可抑制胰腺癌进展[9]。尼妥珠单抗作为单克隆抗体,可减弱或终止EFGR信号转导,发挥抗肿瘤增殖作用[10,11]。且韩春等[12]研究发现,晚期胰腺癌患者分别接受单纯化疗、尼妥珠单抗联合化疗,结果提示胰腺癌晚期患者应用化疗方案与尼妥珠单抗联合治疗可延长中位生存期,且患者可耐受。因此,化疗方案与尼妥珠单抗联合治疗胰腺癌晚期患者不失为较好的选择。
本研究结果显示,观察组临床收益率、总体生存时间较对照组高,说明胰腺癌晚期患者应用尼妥珠单抗联合替吉奥治疗可提高临床收益率,延长生存期。替吉奥是由替加氟、吉美嘧啶、奥替拉西钾组成的复方制剂,经口服给药后替加氟可在机体转化为5-氟尿嘧啶(5-Fu),而5-Fu可阻止脱氧尿甘酸甲基活化为脱氧胸苷酸,干扰肿瘤细胞合成DNA,阻碍肿瘤细胞进行有丝分裂,进而发挥抗肿瘤作用;
吉美嘧啶、奥替拉西钾可对酶发挥抑制作用,维持血液和肿瘤组织中替加氟生成的5-Fu浓度,使5-Fu在血和肿瘤组织中维持时间延长,增强抗肿瘤作用[13,14]。尼妥珠单抗能够与正常细胞和肿瘤细胞上的EGFR进行特异性结合,使EGFR介导的细胞内信号转导通路阻断,减少肿瘤细胞的营养供给,最终抑制机体内肿瘤细胞的增殖与转移,有利于延长患者生存期[15]。同时,尼妥珠单抗还能够直接激活抗体依赖性细胞介导的、补体依赖的细胞的毒性作用,进而杀伤肿瘤细胞,促进其凋亡[16]。因此,胰腺癌晚期患者应用尼妥珠单抗联合替吉奥治疗,可在抑制胸腺嘧啶核苷酸合成酶活性的同时抑制酪氨酸激酶磷酸化,进一步提高临床收益率,延长患者生存期。
安全性方面,对比2组患者不良反应差异不显著,说明胰腺癌晚期患者在替吉奥治疗基础上加用尼妥珠单抗不会明显增加不良反应。究其原因,尼妥珠单抗对EGFR的亲和力中等,能与肿瘤细胞表面EGFR双价结合[17]。同时,尼妥珠单抗的选择性较高,可在体内肿瘤组织中进行高摄取,在正常组织中实现低摄取,减少正常组织损伤,总体毒副作用相对较小,因而不会明显增加胰腺癌晚期患者不良反应[18]。
综上所述,尼妥珠单抗联合替吉奥可提高胰腺癌晚期患者临床收益率,延长生存期,且不增加不良反应。
猜你喜欢吉奥生存期胰腺癌莫瑞吉奥·卡特兰:愿你在此现代装饰(2022年5期)2022-10-13胰腺癌治疗为什么这么难保健医苑(2022年6期)2022-07-08鼻咽癌患者长期生存期的危险因素分析西南国防医药(2016年6期)2016-12-01STAT1和MMP-2在胰腺癌中表达的意义天津医药(2016年9期)2016-10-20胃癌术后患者营养状况及生存期对生存质量的影响癌症进展(2016年11期)2016-03-20术中淋巴结清扫个数对胃癌3年总生存期的影响哈尔滨医药(2015年6期)2015-12-01替吉奥联合紫杉醇治疗晚期胃癌的疗效分析医学研究杂志(2015年5期)2015-06-10单药替吉奥一线治疗老年晚期结直肠癌临床疗效观察西南军医(2015年1期)2015-01-22替吉奥的严重不良反应及应对策略中国药业(2014年19期)2014-05-17健脾散结法联合化疗对56例大肠癌Ⅲ、Ⅳ期患者生存期的影响中医研究(2014年8期)2014-03-11